Fuerza de dispersión de London, Dipolo- inducido.
FUERZA DE DISPERSIÓN DE LONDON
Las fuerzas de
dispersión de London, en honor al científico Fritz London, son unas fuerzas de
tipo intermolecular. Dichas fuerzas tienen lugar entre moléculas de tipo no
polar, donde pueden encontrarse dipolos.
Cuando se representan los orbitales de átomos y moléculas,
la distribución de los electrones, es decir, la densidad electrónica, es el
valor promediado en el tiempo. Lo que da origen a la atracción entre moléculas
vecinas son las oscilaciones respecto a dicho valor promediado en el tiempo.
La forma molecular es un factor más bien secundario, que
afecta a intensidad de las fuerzas de dispersión. Una molécula compacta sólo
permite una pequeña separación de carga, mientras que una molécula alargada
hace posible una separación de carga bastante mayor.
Cuando los electrones están desigualmente distribuidos,
existe un multipolo temporal. Este multipolo interactuará con otros multipolos
cercanos e inducirá a las moléculas, pero sólo son una pequeña parte de la
fuerza de interacción total.
Energía de interacción del dímero de argón. La parte long-range se debe a las fuerzas de dispersión de London.
La densidad electrónica en una molécula puede ser
redistribuida por la proximidad de otro multipolo. Los electrones se acumularán
en el lado de la molécula que encara a la carga positiva y se retirarán de la
carga negativa. Entonces, puede producirse un multipolo transigente por una
molécula polar cercana, o incluso por un multipolo transigente en otra molécula
apolar.
En el vacío, las fuerzas de London son más débiles que otras
fuerzas intermoleculares tales como las interacciones iónicas, el enlace de
hidrógeno, o las interacciones permanentes dipolo-dipolo.
FUERZA DIPOLO-INDUCIDO (INSTANTÁNEO)
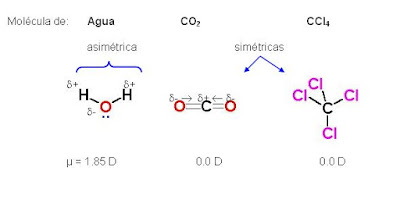
Las fuerzas dipolo-inducido se dan entre moléculas covalentes apolares, e incluso entre
átomos no enlazados, como es el caso de los gases nobles.En las moléculas covalentes apolares, puede suceder que la
nube electrónica, que estará en movimiento constante en torno a los núcleos
atómicos, se halle más desplazada hacia un lado de la molécula durante un
brevísimo lapso de tiempo.
Un enlace no polar es el nombre dado a un enlace en el que
dos átomos comparten electrones de forma igual entre sí.
Estas uniones solamente ocurren cuando dos átomos son de
mismo elemento, dado que solamente los elementos que coinciden tendrán
exactamente la misma capacidad para atraer electrones
Este dipolo instantáneo puede provocar, a su vez, el
desplazamiento de la nube electrónica de las nubes vecinas, formando lo que se
conoce como un dipolo inducido
la intensidad de este tipo de fuerza dependerá de la masa, a
mayor masa molecular mayor fuerza y por lo tanto mayores puntos de fusión y de ebullición

Comentarios
Publicar un comentario