"FUERZAS DE VAN DER
WAALS"
Lo primero que tenemos que saber es que las sustancias químicas son
formadas por moléculas compuestas de átomos, unidos entre sí por medio de
enlaces químicos (covalente, iónico o metálico).
La energía almacenada por estos enlaces, sumada a la red molecular de
todo el conjunto de moléculas que forma la sustancia, determina la estabilidad
de estos enlaces.
Piensa que si en varias moléculas, por ejemplo con enlaces covalente, no
hubiera ninguna fuerza de unión entre ellas, estarían moviéndose libremente y
por lo tanto siempre estarían en estado gaseoso (movimiento libre de las
moléculas).
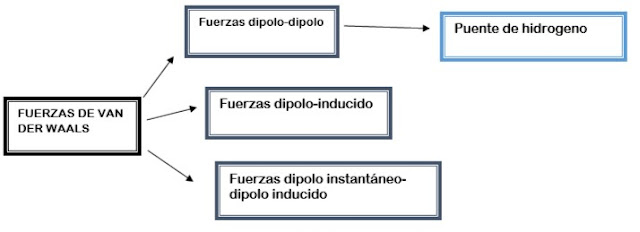
Las fuerzas de van der Waals son fuerzas de estabilización molecular
(dan estabilidad a la unión entre varias moléculas), también conocidas como atracciones
intermoleculares o de largo alcance y son las fuerzas entre moléculas (fuerzas
entre molecula-molecula).
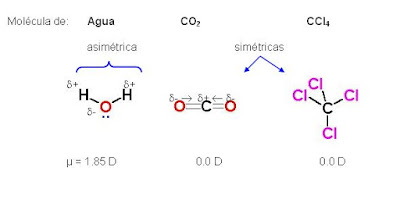
Son fuerzas más débiles que las internas que unen la molécula ya que
dependen exclusivamente del tamaño y forma de la molécula pudiendo ser de
atracción o de repulsión. Son tan débiles que no se las puede considerar un
enlace, como el enlace covalente o iónico, solo se las considera una atracción.
Para tener una idea de la poca fuerza que tienen, si un enlace covalente
tuviera una fuerza de 100, las de Van der Waals serían de valor 1 (100 veces
menor).
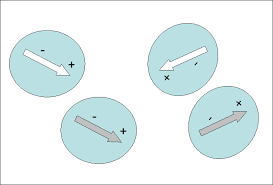
De hecho las fuerzas de van der Waals son las fuerzas atractivas o
repulsivas entre moléculas (o entre partes de una misma molécula) distintas a
aquellas debidas a un enlace (covalente, iónico o metálico). Incluyen a
atracciones entre átomos, moléculas y superficies fuera de los enlaces
normales.

Comentarios
Publicar un comentario